Исследовательская группа под руководством испанских учёных напечатала на 3D-принтере гидрогель, способный имитировать поведение лимфатических узлов человека и ускорять рост Т-клеток у онкологических больных.
Объединив полимер на основе полиэтиленгликоля (ПЭГ) и антикоагулянт гепарина, команда создала структуру, которая позволила Т-клеткам более эффективно мигрировать и пролиферировать. Учитывая, что Т-клетки обладают способностью убивать опухолевые клетки, новый материал исследовательской группы может быть использован в качестве основы для новой формы иммунотерапии рака. Ученые уже подали патент на свой новый полимерный гидрогель в Европейское патентное ведомство и надеются в ближайшем будущем внедрить свою технологию в больницы.
В отличие от химиотерапии и хирургического лечения рака, иммунотерапия использует иммунную систему пациента для защиты от смертельной болезни. Рак может появиться внутри существующих клеток и способен уклоняться от ответа иммунной системы, но Т-клетки могут быть запрограммированы на идентификацию и уничтожение таких клеток с различным уровнем успеха.
Однако подходы, основанные на Т-клетках, сталкиваются с проблемами, поскольку модифицированные клетки сложно производить, манипулировать и контролировать в достаточно больших дозах для эффективной борьбы с раком. Кроме того, лечение, основанное на лимфоцитах, инфильтрирующих опухоль (TIL - Tumor Infiltrating Lymphocytes), которые активно ищут и уничтожают опухоли, крайне нуждается в системах расширения клеток, чтобы стимулировать их более широкое распространение.
Предыдущие исследования в основном были сосредоточены на пролиферации ex vivo Т-клеток, но эти подходы не учитывали влияние лимфатических узлов человека. Цитокин CCL21, например, химическое вещество, присутствующее в лимфатическом узле, взаимодействует с Т-клетками через хемокиновый рецептор CCR7 и усиливает пролиферацию и миграцию клеток.
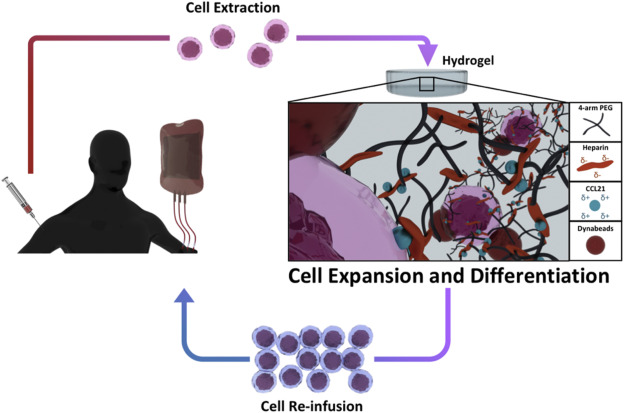
Между тем, внеклеточные матрицы (ECM - Extracellular Matrices) напечатанные на 3D-принтере, часто используются для имитации подлинных ECM и направлены на создание благоприятной среды, которая способствует размножению клеток. В дополнение к обеспечению более реалистичных условий, чем стандартные чашки Петри, изготовленные ЕСМ также могут быть настроены с использованием различных белков и факторов роста для ускорения роста клеток.
Исследователи объединили преимущества CC21, напечатанную в 3D ECM на основе ПЭГ, и гепарина, разжижающего кровь, чтобы создать ECM, который воссоздает условия, существующие в лимфатическом узле. В случае успеха гидрогель команды мог бы активно увеличивать пролиферацию CD4 Т-клеток, одновременно тонко настраивая дифференцировку клеток для адоптивной клеточной терапии (ACT - Adoptive Cell Therapy).
Чтобы создать гидрогель ECM, испанская группа исследователей функционализировала гепарин с помощью химического вещества малеимида. Смесь оставляли на ночь перед очисткой диализом и объединяли с композитом PEG, покрытым физиологическим раствором с фосфатным буфером (PBS - Phosphate Buffered Saline). В результате слияния происходило ковалентное сшивание, что привело к гелеобразованию и, в конечном итоге, к созданию нового гидрогеля.
Позднее были изготовлены ЕСМ с различными массовыми процентами, составляющими 6% масс., 4% масс. и 3% масс. Последующая реология показала, что для стабилизации каждого из них требуется 200-240 минут. Три различных состава были изучены с использованием методов сканирующей электронной микроскопии (SEM), и результаты показали корреляцию между низким количеством PEG и высоким уровнем пористости.
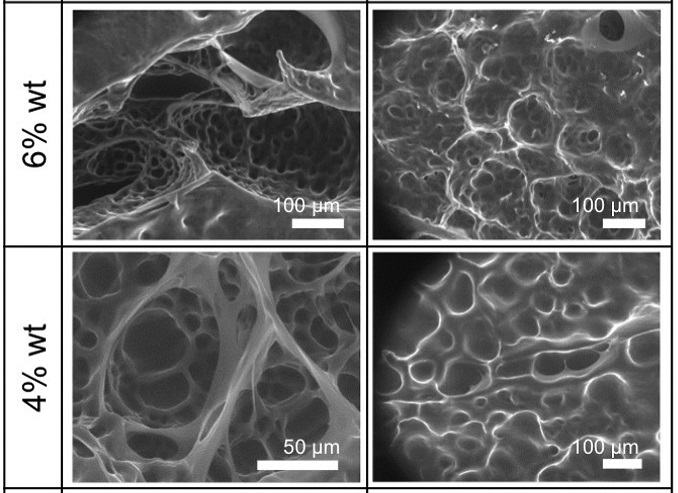
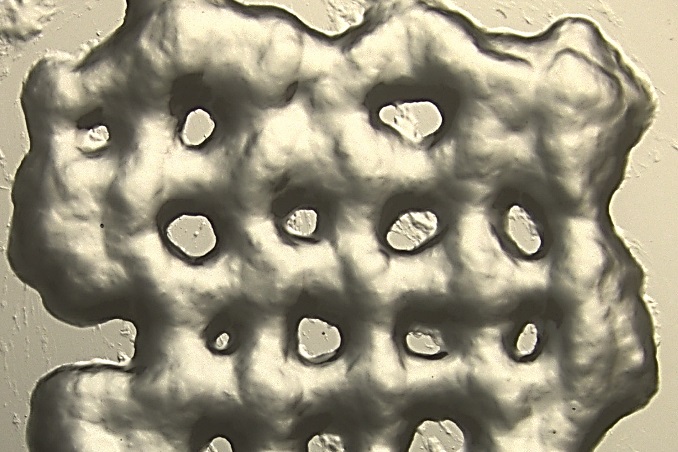
Дальнейший анализ показал, что наблюдаемый средний размер пор составлял 55 мкм, и что ECM с таким уровнем пористости или ниже были бы более благоприятными для расширения клеток, чем более толстые матрицы. В результате 3%-ный гидрогель был идентифицирован как наиболее благоприятный для агрегации и пролиферации Т-клеток. Затем к смеси ЕСМ были добавлены различные концентрации цитокина CC21, 1 нг/мл, 20нг/мл и 100нг/мл, для оценки роста CD4 Т-клеток.
Сводный тест на жизнеспособность пропидия йодида (PI) показал, что Т-клетки реплицировались на 25 процентов больше в PEG-ECM, чем они были бы во взвешенном состоянии ex situ. Было также обнаружено, что нагруженные цитокинами гидрогели способствуют увеличению доли эффекторных клеток, а это означает, что состав Т-клеток может быть изменен в будущем, чтобы повысить их токсичность для раковых клеток.
Исследовательская группа пришла к выводу, что их подход оказался действенной альтернативой методам пролиферации клеток ex vivo. Добавление CCL21 в гидрогель также было продемонстрировано в ходе различных исследований для стимулирования роста клеток. В результате исследователи предположили, что другие химические молекулы, такие как CCL19 и ICAM-1, потенциально могут привести к лучшим клиническим результатам для пациентов при дальнейших исследованиях.
В будущем команда под руководством Испании считает, что их новый гидрогель на основе PEG может найти широкое применение в больницах. «Каркас обеспечивает улучшение пролиферации клеток и влияние на фенотип, что может быть дополнительно изучено для создания искусственных лимфатических узлов», - заявили ученые в своей статье.
«Ожидается, что 3D-гидрогели PEG-Hep с CCL21 будут совместимы с перфузионными системами и новыми биореакторами для работы в условиях надлежащей производственной практики (GMP) на крупных предприятиях», - добавили они.
Каркасы клеток с трехмерной биопечатью в последние годы используются как фармацевтическими компаниями, так и университетскими исследователями для широкого спектра научных инноваций.
Южнокорейская фармацевтическая компания HK inno.N работает с фирмой T&R Biofab, занимающейся трехмерной биопечатью, над тестированием лекарств от кожных заболеваний с использованием биогелевых матриц ECM. Если оценки пройдут успешно, изготовленное мясо можно использовать в качестве альтернативы испытаниям на животных.
Исследователи из Университета Миннесоты разработали новый биогель на основе ECM, позволяющий им создать миниатюрное 3D-печатное бьющееся человеческое сердце. Биоматериал, насыщенный клетками, созданный с использованием плюрипотентных стволовых клеток, позволил им создать более детальную копию аорты.
Ученые из Оксфордского университета и Китайского университета Гонконга разработали новый метод трехмерной биопечати, который позволил им лучше понять, как развивается человеческий мозг. Путем 3D-печати кортикальных клеток человека в мягкий, биосовместимый матригель ВКМ исследователи смогли точно предварительно сформировать из них естественный и неестественный дизайн.
Проект возглавляли исследователи из ICMAB и IBEC в сотрудничестве с VHIO и UIC. Выводы группы подробно описаны в их статье под названием «Изучение метастатического поведения в трехмерной биопечати сосудистой сети для проверки трехмерной вычислительной модели потока», которая была опубликована в журнале Advanced Functional Materials.
