Что, если бы врачи могли просто напечатать почку, используя клетки пациента, вместо того, чтобы искать совместимого донора и надеяться, что тело пациента не отторгнет пересаженную почку?
По словам Дженнифер Льюис, профессора Института биологической инженерии Висса при Гарвардском университете, это может произойти не раньше, чем через десять лет благодаря 3D-биопечати органов. Согласно исследованию 2019 года, биопечать органов — это использование технологий 3D-печати для послойной сборки нескольких типов клеток, факторов роста и биоматериалов для производства биоискусственных органов, которые идеально имитируют свои естественные аналоги.
Этот тип регенеративной медицины находится в стадии разработки, и движущей силой этого новшества является «настоящая человеческая потребность», сказал Льюис.
По данным Управления ресурсов и услуг здравоохранения, по состоянию на 10 июня в США 106 075 мужчин, женщин и детей находятся в национальном списке ожидания на трансплантацию органов. Однако живые доноры предоставляют в среднем только около 6000 органов в год, и ежегодно насчитывается около 8000 умерших доноров, каждый из которых предоставляет в среднем 3,5 органа.
Причиной этого несоответствия является «сочетание людей, которые переживают катастрофические события со здоровьем, но их органы недостаточно высокого качества для донорства, или они изначально не внесены в список доноров органов, и тот факт, что это на самом деле очень трудно найти подходящую пару», чтобы тело пациента не отторгало пересаженный орган, сказал Льюис.
И хотя живые доноры являются вариантом, «делать операцию тому, кто в ней не нуждается», — это большой риск, сказал доктор Энтони Атала, директор Института регенеративной медицины Уэйк Форест. «Таким образом, живые родственные доноры обычно не являются предпочтительным путем, потому что тогда вы забираете орган у кого-то ещё, кому он может понадобиться, особенно сейчас, когда мы стареем дольше».
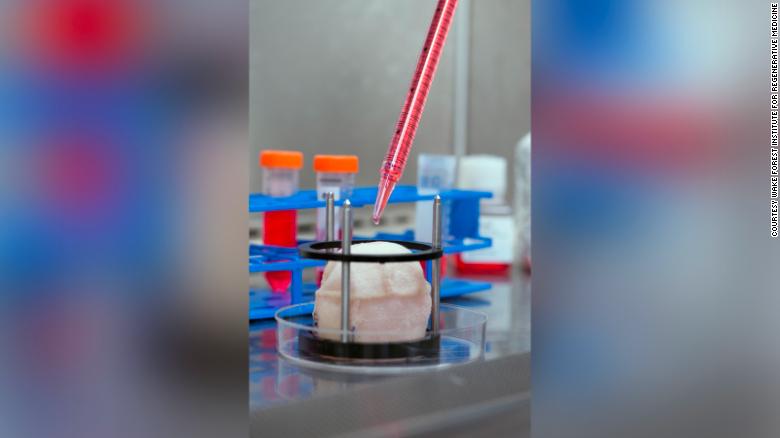
Атала и его коллеги были ответственны за выращивание человеческих мочевых пузырей в лаборатории вручную в 2006 году и впервые имплантировали людям сложный внутренний орган, спасая жизни троих детей, которым они имплантировали мочевые пузыри.
По данным Управления ресурсов и услуг здравоохранения, каждый день 17 человек умирают в ожидании трансплантации органов. И каждые девять минут в список ожидания добавляется еще один человек, сообщает агентство. Более 90% людей из списка на трансплантацию в 2021 году нуждались в почках.
«Около миллиона человек во всем мире нуждаются в почке. Таким образом, у них терминальная стадия почечной недостаточности, и они должны пройти диализ», — сказал Льюис. «После того, как вы переходите на диализ, вам остается жить пять лет, и каждый год уровень вашей смертности увеличивается на 15%. Диализ очень тяжел для вашего тела. Так что это действительно мотивирует взяться за эту грандиозную задачу печати органов."
«Антигипертензивные таблетки не являются дефицитом. Каждый, кто в них нуждается, может их получить», — заявила Мартин Ротблатт, генеральный директор и председатель United Therapeutics, на конференции Life Itself, мероприятии, посвященном здоровью и благополучию, представленному в партнерстве с CNN. United Therapeutics является одним из спонсоров конференции.
«Нет никакой практической причины, по которой любой, кому нужна почка — или легкое, сердце, печень — не сможет их получить», — добавила она. «Мы используем технологии, чтобы решить эту проблему».
Чтобы начать процесс биопечати органа, врачи обычно начинают с собственных клеток пациента. Они берут биопсию органа с помощью небольшой иглы или выполняют минимально инвазивную хирургическую процедуру, при которой удаляется небольшой кусочек ткани, «меньше половины размера почтовой марки», — сказал Атала. «Взяв этот небольшой кусочек ткани, мы можем разделить клетки (и) вырастить и расширить клетки вне тела».
Этот рост происходит в стерильном инкубаторе или биореакторе, сосуде из нержавеющей стали под давлением, который помогает клеткам питаться питательными веществами, называемыми «средами». Врачи кормят их каждые 24 часа, поскольку клетки имеют собственный метаболизм, сказал Льюис. По словам Атала, каждый тип клеток имеет свою среду, и инкубатор или биореактор действует как устройство, похожее на печь, имитирующее внутреннюю температуру и насыщение кислородом человеческого тела.
«Затем мы смешиваем его с этим гелем, который похож на клей», — сказал Атала. «Каждый орган в вашем теле имеет клетки и клей, который удерживает их вместе. По сути, это также называется «внеклеточным матриксом»."
 По словам Льюиса, этот клей — прозвище Atala для биочернил, пригодный для печати смеси живых клеток, богатых водой молекул, называемых гидрогелями, а также среды и факторов роста, которые помогают клеткам продолжать размножаться и дифференцироваться. Гидрогели имитируют внеклеточный матрикс человеческого тела, который содержит такие вещества, как белки, коллаген и гиалуроновая кислота.
По словам Льюиса, этот клей — прозвище Atala для биочернил, пригодный для печати смеси живых клеток, богатых водой молекул, называемых гидрогелями, а также среды и факторов роста, которые помогают клеткам продолжать размножаться и дифференцироваться. Гидрогели имитируют внеклеточный матрикс человеческого тела, который содержит такие вещества, как белки, коллаген и гиалуроновая кислота.
Часть клея, не содержащая клеток, может быть изготовлена в лаборатории и «будет иметь те же свойства ткани, которую вы пытаетесь заменить», — сказал Атала.
По словам Льюиса, используемые биоматериалы обычно должны быть нетоксичными, биоразлагаемыми и биосовместимыми, чтобы избежать отрицательного иммунного ответа. Коллаген и желатин являются двумя наиболее распространенными биоматериалами, используемыми для биопечати тканей или органов.
Затем врачи загружают каждый сорт биочернил — в зависимости от того, сколько типов клеток они хотят напечатать — в камеру для печати, «используя печатающую головку и сопло для выдавливания чернил и создания материала слой за слоем», — сказал Льюис. По словам Атала, создание тканей с персонализированными свойствами возможно благодаря тому, что принтеры программируются с использованием данных изображений пациента, полученных с помощью рентгеновских лучей или сканов.
«С цветным принтером у вас есть несколько разных картриджей, и каждый картридж печатает свой цвет, и вы выбираете свой (окончательный) цвет», — добавил Атала. Биопечать такая же, вы просто используете ячейки вместо традиционных чернил.
По словам Льюиса, продолжительность процесса печати зависит от нескольких факторов, в том числе от печатаемого органа или ткани, точности разрешения и количества необходимых печатающих головок. Но обычно это длится от нескольких до нескольких часов. По словам Атала, время от биопсии до имплантации составляет от четырех до шести недель.

Конечная задача состоит в том, чтобы «заставить органы действительно функционировать так, как они должны», поэтому достижение этого «является Святым Граалем», сказала Льюис. «Точно так же, как если бы вы собирали орган у донора, вы должны немедленно поместить этот орган в биореактор и начать перфузию, иначе клетки умрут», — добавила она. Перфузировать орган означает снабжать его жидкостью, обычно кровью или кровезаменителем, путем ее циркуляции по кровеносным сосудам или другим каналам.
По словам Льюиса, в зависимости от сложности органа иногда возникает необходимость дальнейшего созревания ткани в биореакторе или дополнительных соединений. «Есть просто ряд проблем с сантехникой, которые необходимо решить, чтобы заставить этот напечатанный орган действительно функционировать так же, как человеческий орган в естественных условиях (имеется в виду в теле). И, честно говоря, это еще не решено полностью».
Как только биопечатный орган будет имплантирован пациенту, он со временем естественным образом деградирует — и это нормально, поскольку он предназначен для такой работы.
«Вы, наверное, задаетесь вопросом: «Ну, а что тогда происходит с тканью? Она развалится?» На самом деле нет», — сказал Атала. «Эти клеи растворяются, и клетки чувствуют, что мост рушится; они чувствуют, что у них больше нет прочной опоры, их собственный клей».
Атала и Льюис консервативны в своих оценках количества лет, оставшихся до того, как полностью функционирующие биопринтированные органы можно будет имплантировать людям. «Область развивается быстро, но я имею в виду, я думаю, что мы говорим о десятилетии с лишним, даже несмотря на весь достигнутый огромный прогресс», — сказал Льюис.
«Много лет назад я научился никогда не предсказывать, потому что всегда ошибаешься», — сказал Атала. «Существует так много факторов с точки зрения производства и (регулирования Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США). В конце концов, наш интерес, конечно же, состоит в том, чтобы убедиться, что технологии прежде всего безопасны для пациента».
Всякий раз, когда биопечать органов становится доступным вариантом, доступность для пациентов и тех, кто за ними ухаживает, не должна быть проблемой.
Они будут «наверняка доступны», — сказал Атала. «Затраты, связанные с отказами органов, очень высоки. Только содержание одного пациента на диализе стоит более четверти миллиона долларов в год. Таким образом, намного дешевле создать орган, который вы можете имплантировать в пациента».
Согласно исследованию, опубликованному Американским обществом нефрологов, в 2020 году средняя стоимость трансплантации почки составляла 442 500 долларов, в то время как 3D-принтеры продаются по цене от нескольких тысяч до 100 000 долларов, в зависимости от их сложности. Но даже несмотря на то, что доступны недорогие принтеры, дорогостоящие части биопечати могут включать в себя поддержание банков клеток для пациентов, культивирование клеток и безопасное обращение с биологическими материалами, сказал Льюис.
Некоторые из основных расходов на текущую трансплантацию органов включают «извлечение органа у донора, транспортные расходы и, конечно же, операцию, которую проходит реципиент, а затем весь уход и мониторинг», — сказал Льюис. «Некоторые из этих затрат всё ещё были бы в игре, даже если бы они были напечатаны биопринтом».
