Глобальная сертификационная компания TÜV SÜD выпустила первое в отрасли руководство по 3D-печати для многократного производства медицинских продуктов, которые являются безопасными и пригодными для использования.
В руководстве компании, опубликованном в виде официального документа, изложены стандарты, которым производители должны соответствовать на каждом этапе рабочего процесса, а также полномочия, необходимые для их применения. Сводя соответствующие правила в упрощенный формат, TÜV SÜD заявляет, что стремится «наметить возможные процедуры» и «указать на существующие пробелы» для тех, кто работает как в области 3D-печати, так и в клинических условиях.

Согласно TÜV SÜD, стандартизация аддитивного производства серьезно началась только недавно, но, учитывая потенциальную гарантию качества и повышение производительности, к ней стоит стремиться. Хотя стандарты ISO 9001 и 13485 часто используются в медицинском производстве и представляют собой надежные системы управления качеством (QMS), они не решают уникальные проблемы 3D-печати, характерные для конкретного сектора.
Вот почему TÜV SÜD опубликовал собственную цепочку процессов, от квалификации до постобработки, в которой подчеркиваются шаги, которые необходимо предпринять производителям, чтобы соответствовать требованиям при 3D-печати медицинских деталей. Фирма заявляет, что перед началом производства «технически компетентный человек» должен проверить требования в отношении биосовместимости и стерильности, которым должны соответствовать любые созданные детали.
После определения всех нормативных требований сам производственный процесс должен быть квалифицирован или утвержден, что является стандартом для индустрии 3D-печати. Тем не менее, именно в этом рабочий процесс TÜV SÜD отличается тем, что он разделяет квалификацию на «концептуальную» и «основную проверку процесса». Подвергая свои процессы такой тщательной проверке, компания заявляет, что пользователям «практически гарантированы» качественные результаты.
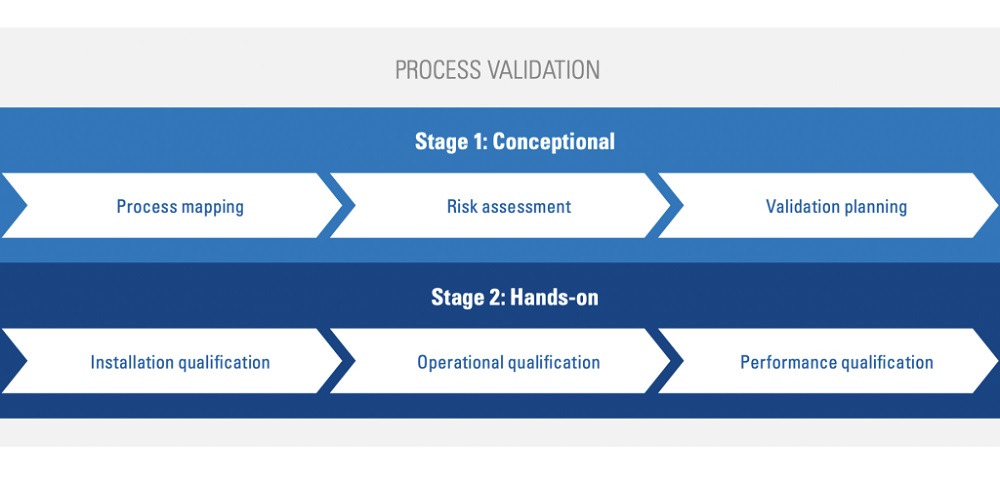
Концептуальная фаза рабочего процесса фирмы начинается с составления карты процесса, во время которого производителям предлагается полностью перечислить входные и выходные параметры для выявления любых потенциальных рисков или пробелов в эффективности. Затем следует провести оценку риска, которую TÜV SÜD рекомендует проводить в соответствии с общим процессом ISO 14971, а также диаграммой Исикавы или анализом дерева отказов.
После того, как оценка рисков завершена и производители определили все средства предотвращения выхода из строя или загрязнения отпечатков, компания предлагает перейти на этап «планирования валидации». В этом процессе пользователи создают четкую дорожную карту того, что необходимо проверить, в дополнение к предполагаемым методам тестирования, для которых все соответствующее оборудование должно быть указано на соответствие.
Наконец, на этапе практической «основной проверки» производители должны провести процедуры установки, эксплуатации и аттестации рабочих характеристик. Хотя подробности этих шагов полностью изложены в документе фирмы, она широко рекомендует применять ISO/ASTM 52920 во время аттестации и ISO/ASTM 52904 в отношении LPBF.
В соответствии со своим стремлением обеспечить непрерывную гарантию качества, руководство TÜV SÜD также включает рекомендации по постобработке медицинских деталей, напечатанных на 3D-принтере. Фирма утверждает, что обработка компонентов может резко повлиять на их соответствие, поэтому производители должны придерживаться серии ISO 10993 при очистке, стерилизации и упаковке, чтобы избежать нарушения биологической безопасности.
Перед упаковкой такие медицинские продукты часто подвергаются испытаниям, которые оценивают их цитотоксичность, эффекты имплантации, гемосовместимость и канцерогенность. После того, как они будут завершены, TÜV SÜD предлагает производителям следовать стандартам EN 556 и ISO 11607, чтобы гарантировать, что все продукты поступают на рынок без ущерба для их свойств, при этом делая это «с максимальной осторожностью».
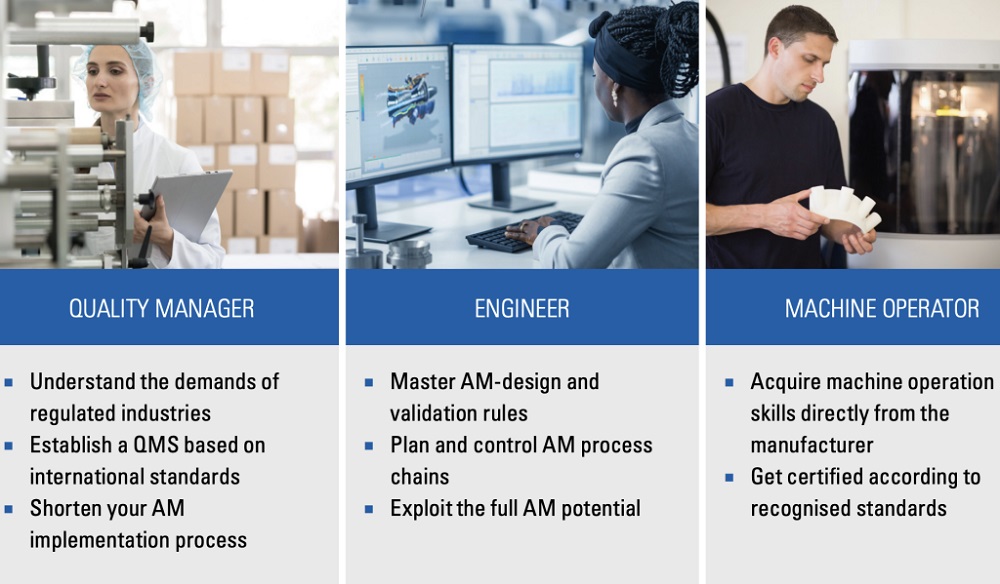
Хотя этот этап завершает рабочий процесс компании, соответствующий требованиям безопасности, он также опубликовал руководство, в котором описаны навыки, необходимые для эффективного выполнения этих этапов обработки. В своем документе TÜV SÜD подчеркивает, что ручной характер многих процессов 3D-печати означает, что «персонал играет решающую роль в качестве продукции», поэтому они должны иметь уровень подготовки, установленный такими стандартами, как ISO/ASTM CD 52926-1. .
Фактически, эти стандарты ISO утверждают, что инженеры, испытательный персонал и какой-либо руководитель необходимы для 3D-печати рыночной медицинской продукции. Хотя компания заявляет, что все роли нуждаются в «глубоком понимании» 3D-печати, она сохраняет тот факт, что персонал должен обладать знаниями и в других областях, чтобы они могли вносить свой вклад в планы валидации и позволять производить «высококачественные устройства».
Для получения дополнительной информации о процессе медицинской 3D-печати TÜV SÜD, в том числе о соблюдении требований будущих стандартов ISO, читатели могут получить доступ к полному тексту статьи здесь.

TÜV SÜD со своей базой в Мюнхене, Германия, является поставщиком технических услуг, специализирующимся на оценке передовых процессов. За последние несколько лет компания сыграла важную роль в работе с фирмами, занимающимися 3D-печатью, над установлением отраслевых стандартов, позволяющих производителям сертифицировать продукцию, чтобы повысить доверие к ним на рынке.
Например, в сентябре 2020 года TÜV SÜD намеревалась уточнить нормативные требования, касающиеся 3D-печатных СИЗ, после массового использования технологии для производства масок из-за пандемии COVID-19. Для этого компания опубликовала медицинские контрольные списки для 3D-печати, которые помогли производителям обеспечить соблюдение соответствующих стандартов безопасности и качества.
Компания также запустила собственные специализированные учебные курсы по соблюдению требований безопасности в 3D-печати. Цифровая обучающая платформа, состоящая из восьми онлайн-модулей, предназначена для предоставления инженерам аддитивного производства курсов повышения квалификации по стандартам DIN, ISO и ASTM, касающимся производственной безопасности, управления рисками и качеством.
TÜV SÜD участвует не только в разработке руководства, но и в обеспечении его соблюдения, и в ноябре прошлого года он завершил свой первый в истории комбинированный аудит 3D-печати на автоспортивной фирме Sauber Engineering. В ходе визита, проводимого в рамках услуги компании «Сертификация производственных площадок Industrial AM», компания Sauber Engineering получила сертификаты соответствия ISO 9001 и DIN SPEC 17071.
